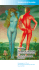Der Herpes genitalis
Transcription
Der Herpes genitalis
M E D I Z I N DIE ÜBERSICHT Der Herpes genitalis Eiko E. Petersen1, Hans W. Doerr2, Gerd Gross3, Detlef Petzoldt 4, Ernst Rainer Weissenbacher 5, Peter Wutzler 6 ZUSAMMENFASSUNG Der Herpes genitalis wird vor allem durch den Herpessimplex-Virus Typ 2, aber zunehmend auch durch den oralen Typ 1 verursacht. Charakteristisch für die sexuell übertragene Ersterkrankung ist die Streuung der Bläschen und Erosionen über weite Teile des Genitales und die Schmerzhaftigkeit auch der vergrößerten Leistenlymphknoten. Bei frühzeitiger Diagnose kann der Verlauf durch eine orale antivirale Therapie erheblich abgekürzt werden. Bei rezidivierenden Schmerzen im Genitalbereich sollte immer an die Möglichkeit eines rezidivierenden Herpes genitalis gedacht werden, der gewöhnlich milder verläuft, da er nur an einer Stelle auftritt, die aber wechseln kann. Bei frühzeitiger Diagnose kann eine orale Therapie den Verlauf auch verkürzen. Die Diagnose wird durch den Erregernachweis gesichert. Die Serologie ist nur für den Immunstatus und den Herpesausschluß geeignet. Die Kinder seronegativer Mütter sind peripartal besonders gefährdet, da dann eine schwere Primärerkrankung über die Mutter oder durch Besuch möglich ist. Schlüsselwörter: Herpes genitalis, Primärerkrankung, Behçet-Syndrom, Neugeborenenherpes Genital Herpes Virus Infection Sexually transmitted herpes virus infections are mainly due to herpes simplex virus (HSV) type 2, increasing rates of infections with HSV type 1 occur. Primary disease can be very painfull with inflammation, dysuria and fever as well as widespread vesicles and erosions. Recurrent endogenous reactivations of genital herpes develop with a less severe course. Both forms may be suppressed by early virostatic therapy. Genital herpes which is transmitted to the newborn by an infected mother during birth may take a disastrous course. Prevention is possible with prepartal virostatic treatment of the mother or by cesarian section. The most reliable diagnosis of HSV is the direct detection of the pathogen. Key words: Genital herpes, primary disease, Behçet syndrome, herpes of the newborn D er Herpes genitalis ist eine sexuell übertragbare Viruserkrankung. Die Primärinfektion kann schwer verlaufen. Rezidive mit wechselnden Beschwerden können sehr lästig sein. Die Übertragung des Virus auf das Neugeborene kann zu einer fatalen Infektion führen. Das klinische Bild ist wechselnd und reicht von der asymptomatischen Virusausscheidung über brennende Schmerzen und einer schmerzhaften fiebrigen Vulvitis beziehungsweise Balanoposthitis bis hin zur Enzephalitis. Der Grad der Belästigung hängt ab von Häufigkeit und Ausmaß der lokalen Entzündungsreaktion. Eine frühzeitige Therapie kann sowohl Häufigkeit wie Ausmaß senken. Wegen der Variabilität der Rezidivfrequenz und der Beschwerden werden viele rezidivierende Herpesattacken als solche nicht erkannt. Auf der anderen Seite werden vermeintliche durch den Herpesvirus verursachte Ulzera erfolglos therapiert, was zu Zweifeln an der Therapie führt. Erreger Der Herpes genitalis kann durch die Infektion zweier humanpathogener Herpesviren hervorgerufen werden (5, 19), und zwar durch Infektionen mit dem Herpes-simplex-Virus Typ 2 (HSV 2) und dem Herpes-simplex-Virus Typ 1 (HSV 1). Ihr Genom besteht aus einer linearen doppelsträngigen DNA. Das Nukleokapsid wird von einer lockeren Hülle aus 1 Sektion Gynäkologische Infektiologie (Leiter: Prof. Dr. med. Eiko E. Petersen), AlbertLudwigs-Universität, Freiburg 2 Institut für medizinische Virologie (Direktor: Prof. Dr. med. Hans W. Doerr), Johann Wolfgang Goethe-Universität, Frankfurt/Main 3 Klinik für Dermatologie und Venerologie (Direktor: Prof. Dr. med. Gerd Gross), Universität Rostock 4 Hautklinik (Direktor: Prof. Dr. med. Detlef Petzoldt), Ruprecht-Karls-Universität, Heidelberg 5 Universitäts-Frauenklinik (Direktor: Prof. Dr. med. H. Hepp), Ludwig-Maximilians-Universität, München 6 Institut für antivirale Chemotherapie (Direktor: Prof. Dr. med. habil. Peter Wutzler), FriedrichSchiller-Universität, Erfurt A-2358 (46) Deutsches Ärzteblatt 96, Heft 38, 24. September 1999 SUMMARY Phosphoproteinen eingehüllt (Tegument). Das Genom von Herpes-simplex-Virus Typ 1 und 2 hat zu etwa 50 Prozent homologe Nukleotidsequenzen. Serologisch können die beiden Viren anhand verschiedener Antigene auf dem Nukleokapsid und besonders auf dem Envelope mittels spezifischer monoklonaler Antikörper unterschieden werden (25). Der Mensch scheint das einzige natürliche Reservoir für diese Viren zu sein. HSV 1 gilt als der orale Typ, der hier nahezu ausschließlich gefunden wird, während HSV 2 als genitaler Typ definiert wird. Übertragung Diese erfolgt durch Schmierinfektion von Mensch zu Mensch. Über Gegenstände wird die Infektion wegen der Labilität des Virus nur selten übertragen. Im Einzelfall ist dies jedoch möglich. Eintrittspforten sind die Schleimhaut und kleine Hautverletzungen der verhornten äußeren Haut. Menge des übertragenen Virus, Eintrittspforte M E D I Z I N DIE ÜBERSICHT Foto: Gross weis möglich ist. Selbst im Krustenstadium läßt sich noch Virus kulturell nachweisen. Auch ohne sichtbare Läsionen können Herpesviren ausgeschieden werden, zum Beispiel im Bereich der Zervix, der Urethra und des Mundes, und so der Sexualpartner oder das Neugeborene infiziert werden (34). Dies scheint sogar die häufigste Form der Infektionsübertragung auf den Sexualpartner zu sein. Petting schützt nicht sicher vor Übertragung und auch das Kondom ist nur ein teilweiser Schutz, da es nicht den ganzen Genitalbereich bedeckt. Foto: Petersen 80 bis 90 Prozent der Erwachsenen besitzen Antikörper gegen Herpes-simplex-Viren, wobei sich bei zirka einem Viertel auch/oder Antikörper gegen den Typ 2 nachweisen lassen. Die Primärinfektion erfolgt meist im Kleinkindalter im Orofazialbereich an Haut- oder Schleimhautgrenzen durch HSV 1. Die Infektion wird durch Körperkontakt, gewöhnlich schon im Kleinkindalter, übertragen. 50 Prozent aller Kinder werden mit dem Virus infiziert und sind dann seropositiv. Nur selten kommt es zur klinischen Manifestation (Stomatitis aphthosa, Herpes corneae). Ein zweiter Durchseuchungsschub beginnt im postpubertären Alter mit Intimpartnerschaften. Erst zu diesem Zeitpunkt tritt auch das HSV 2 epidemiologisch in Erscheinung. Erwachsene haben zu zirka 70 bis 80 Prozent Antikörper gegen HSV 1 und zu zirka 20 bis 30 Prozent gegen HSV 2 (3, Abbildung 3: Gleiche Patientin wie Abbildung 2, drei 9, 22, 25). Möglicherweise besteht zwi- Tage nach Therapiebeginn schen HSV 1 und 2 eine partielle Kreuzimmunität, welche die Ausbreitung des HSV 2 behindert (4). Die in den Vereinigten Staaten (9) beobachtete starke Zunahme der HSV-2-IgGSeroprävalenz um 30 Prozent seit dem Jahr 1970 konnte in Deutschland noch nicht gezeigt werden, da die epidemiologischen Daten fehlen. Allgemeine Untersuchungen aus den letzten Jahren haben Abbildung 4: Leistenlymphknoten-Schwellung bei Patientin mit gezeigt, daß bei uns, insbeson- primärem Herpes genitalis Abbildung 2: Primärer Herpes genitalis durch HSV 1 bei einer 20jährigen Frau mit ausgeprägtem Ödem, Knötchen und Bläschen und Immunstatus des Betroffenen sind entscheidend für die Dauer der Inkubationszeit und die Schwere der nachfolgenden Erkrankung. Infektiosität Mit Viruspartikeln angefüllte Bläschen sind besonders infektiös. Auch aus den Ulzera beziehungsweise Erosionen wird viel Virus freigesetzt, so daß hieraus der Erregernach- Foto: Petersen Foto: Petersen Pathogenese Während der aktiven Infektion gelangt das HSV beim Herpes genitalis über sensorische Nervenbahnen in das sacrospinale Hinterwurzel- Epidemiologie Abbildung 1: Primärer Herpes genitalis beim Mann dere bei Frauen, der Anteil HSV-1-bedingter Genitalisfälle ansteigt. Etwa 70 bis 80 Prozent der genitalen Herpesattacken werden von HSV 2, 20 bis 30 Prozent von HSV 1 verursacht. Bei den klinisch manifesten Primärinfektionen wird heute in zirka 50 Prozent der Fälle HSV 1 isoliert. Der Manifestationsindex der primären Genitalinfektion ist nicht genau bekannt. Er wird auf zirka 20 bis 30 Prozent geschätzt. Deutsches Ärzteblatt 96, Heft 38, 24. September 1999 (47) A-2359 M E D I Z I N DIE ÜBERSICHT Foto: Petersen Abbildung 5: Primärer Herpes genitalis auf der Portio bei 18jähriger Patientin Wichtige Streßfaktoren sind: Hormonelle Umstellung (menstruationsassoziierter Herpes), psychische Belastung (Ärger, Erschöpfung, Schlafentzug), traumatische Noxen, UV-Lichtbestrahlung des mukokutanen Innervations-Segmentes, Infektionen und Fieber (Herpes febrilis). Klinisches Bild des Herpes genitalis Nur 30 Prozent der Fälle von Herpes genitalis manifestieren sich klinisch eindeutig. 50 Prozent verlaufen völlig asymptomatisch, die restlichen 20 Prozent machen zwar Symptome, die aber vom Patienten, manchmal auch vom Arzt, falsch gedeutet werden. Die tatsächliche Zahl der HSV-2-infizierten Patienten in der Praxis liegt somit mehr als dreimal so hoch, wie man aufgrund des klinischen Eindruckes schätzen würde. Das klinische Bild ist sehr typisch. Immer läuft die Infektion in ganz bestimmten Stadien ab, wobei diese unterschiedlich in Ausprägung und Dauer sein können. Grundsätzlich unterscheiden wir zwei Formen beim Herpes genitalis: c exogene Primärinfektion, c endogene Reaktivierung des persistierenden Virus. Für die Primärinfektion sind meist Sexualkontakte direkt oder indirekt notwendig. Sie wird daher zu den sexuell übertragenen Infektionen (STD) gezählt. Das Rezidiv erfolgt unabhängig von Sexualkontakten und ist eine endogene Reaktivierung. Auch klinisch unterscheiden sich beide Erkrankungsformen. Foto: Petersen ganglion, wo es nach Abheilung der größeren oder auch nur minimalen Primärentzündung latent persistiert. In dieser Phase kann in den Neuronen kein virales Strukturprotein, sondern nur das Genom und latenzassoziierte Regulatorproteine molekularbiologisch nachgewiesen werden. Durch verschiedene Streßfaktoren wird die latente Infektion zu einer virusproduktiven Infektion reaktiviert. Abbildung 7: Herpes urethralis, fälschlich als Zystitis behandelt Mehr als zwei Drittel der Patienten haben systemische Erscheinungen, wie Fieber, Kopfschmerzen, Krankheitsgefühl oder Muskel- und Rückenschmerzen. Die lokalen Erscheinungen sind weniger ausgedehnt und die systemischen Erscheinungen kommen seltener vor bei Patienten, die bereits über HSV-1-Antikörper verfügen, meist aufgrund einer in der Kindheit durchgemachten oralen Herpesinfektion. Abbildung 6: Herpes-genitalis-Rezidiv bei 45jähriger Patientin Die Inkubationszeit beträgt drei bis sieben Tage, eventuell länger. Klinische Charakteristika einer Primärerkrankung sind: c die Aussaat der Bläschen über größere Flächen des Genitale und der angrenzenden Haut (Abbildungen 1 bis 3), c die Beidseitigkeit der Erscheinungen (Abbildungen 2 bis 3), c die lange Bestandsdauer der Läsionen bis zu drei Wochen. A-2360 (48) Deutsches Ärzteblatt 96, Heft 38, 24. September 1999 Foto: Petersen Foto: Petersen Primärer Herpes genitalis Abbildung 8: Behçet-Syndrom bei einer 29jährigen Schwangeren in der 12. SSW M E D I Z I N DIE ÜBERSICHT Etwa 50 Prozent der primären Herpes-genitalis-Erkrankungen werden beim ersten Arztbesuch nicht diagnostiziert, da es zunächst nur brennt und schmerzt und in diesem frühen Stadium noch keine Bläschen oder Erosionen sichtbar sind. Häufig wird die Frühform mit einer Candidose (Pilzinfektion) verwechselt. Dolente Leistenlymphknotenschwellung beidseits (Abbildung 4) ist ein weiteres typisches Zeichen eines primären Herpes genitalis. Neben dem Vulvabereich können auch der Vaginalbereich und die Portio (Abbildung 5) betroffen sein. Wegen der Schmerzhaftigkeit des empfindlichen Vulvabereichs bei starker Ausprägung ist eine Spekulumeinstellung zunächst meist nicht möglich. Ausgedehnter primärer Herpes genitalis des Vulvabereichs beim Kind ist selten und nur durch Schmierinfektion von der Mutter oder durch sexuellen Mißbrauch möglich. Die primäre Manifestation der HSV-Infektion im Genitalbereich kann gefolgt sein von einer Reihe unterschiedlicher Komplikationen wie extragenitale Herde, zum Beispiel an Fingern (Herpes Paronychie), am Auge (Keratoconjunctivitis herpetica), Oropharyngealbereich (5). Die Ursache ist hier in der Regel eine vom Genital ausgehende Schmierinfektion (Autoinokulation). Miktionsbeschwerden im Rahmen des primären Herpes genitalis können unter anderem auf Herpesbläschen in Urethranähe zurückgeführt werden. Auch eine direkt durch HSV induzierte Dysfunktion des autonomen Nervensystems wird diskutiert. Eine spontane benigne Meningitis wird häufiger bei Frauen (36 Prozent) als bei Männern (13 Prozent) beobachtet (5). Bei Fieber und Kopfschmerzen, Verhaltensauffälligkeiten und Krämpfen muß eine Herpesenzephalitis ausgeschlossen werden. Eine schwere Komplikation, besonders bei Männern, ist die im Verlauf einer herpetischen Proktitis auftretende sakrale Radikulomyelopathie mit Befall sensorischer und autonomer Nerven. Die Prognose ist günstig. Die Abheilung erfolgt innerhalb von zwei bis vier Wochen (4, 15). Rezidivierender Herpes genitalis Dem primären Herpes genitalis folgt bei zirka 85 Prozent aller Patienten ein symptomatisches Rezidiv (19). Meistens handelt es sich um umschriebene, gruppierte Bläschen und Erosionen (Abbildung 6). Winzige Erosionen können oft nur über Schmerzlokalisation mittels Lupe oder Kolposkop aufgespürt werden. Allgemeine Symptome sind hier seltener als bei der Primärinfektion. Dies trifft auch auf regionale Lymphknotenschwellungen und neuralgische Beschwerden zu. Die Rezidivhäufigkeit schwankt und beträgt in Abhängigkeit vom HSV-Typ bis zu Differentialdiagnosen des Herpes genitalis c Vulvitis pustulosa durch Candida albicans c Behçet-Syndrom c Trichomoniasis c Verletzungen nach Kohabitation, Kratzen bei Juckreiz c Vulvitis/Balanitis Plasmacellularis c Varizellen beziehungsweise Zoster c Pemphigus vulgaris, bullöses Pemphigoid c Herpes gestationis c Mollusca contagiosa c Lues (Primäraffekt) c Urethritis c Proktitis c Kontaktdermatitis zwölf und mehr Rezidive pro Jahr, wobei HSV-2-Rezidive häufiger sind als HSV-1-Rezidive. Im Gegensatz zur Primärmanifestation wird das Herpesrezidiv im Genitalbereich von prodromalen Beschwerden wie Hyperästhesie, neuralgieähnlichen Schmerzen und Krankheitsgefühl angekündigt. Insbesondere der rezidivierende Herpes kann ernstzunehmende emotionale, sexuelle und psychosoziale Konflikte in einer bestehenden Partnerschaft auslösen. Nicht selten wird der Herpes mit einer rezidivierenden Zystitis verwechselt. Die Abbildung 7 zeigt einen Herpes urethralis bei einer Patientin, die zehn Jahre lang immer wieder wegen Zystitis mit Antibiotika behandelt wurde. Gelegentlich, wenn die bakteriologische Kultur aus dem Urin negativ war, wurden ihre Beschwerden auch als psychosomatisch bedingt abgetan. Die Viruskultur ergab HSV 2. Die frühzeitige Einnahme von Aciclovir-Tabletten hat die Patientin von ihrem sie sehr belastenden Problem weitgehend befreit. Herpesherde können auch in der Vagina und auf der Portio lokalisiert sein. Wegen der geringen Sensibilität dieser Areale wird der allein hier ablaufende Herpes nur als Zufallsbefund entdeckt. Allenfalls kann einmal stärkerer Ausfluß auftreten, als dessen Ursache der Herpes auch nur dann entdeckt wird, wenn die Vagina sorgfältig abgesucht wird und entsprechende Nachweisverfahren angewendet werden. Neugeborenenherpes Eine Herpes-simplex-Infektion beim Neugeborenen ist eine seltene, aber meist sehr schwere Erkrankung mit einer hohen Mortalität. Da Hauteffloreszenzen oft sehr spät auftreten, kommt die mögliche Therapie häufig zu spät. Nur wenn das Risiko bekannt ist und Frühzeichen beim Neugeborenen beachtet werden, sind die Chancen gut. Das höchste Risiko (zirka 33 Prozent) für das Neugeborene besteht bei einer Primärinfektion der Mutter unmittelbar vor der Entbindung (5, 16, 19, 32). Dies ist zum Glück ein sehr seltenes Ereignis. Dagegen ist die asymptomatische Virusausscheidung der Mutter unter der Geburt nicht so selten und wird zwischen 0,1 und 0,5 Prozent aller Schwangerschaften beziehungsweise bei ein Prozent der Frauen mit bekanntem rezidivierenden Herpes genitalis angenommen. Eine primäre Schnittentbindung muß beim primären Herpes genitalis immer durchgeführt werden. Beim Herpesrezidiv gibt es erste Erfahrungen mit vaginaler Entbindung unter einer Aciclovir-Behandlung, die zu einer Deutsches Ärzteblatt 96, Heft 38, 24. September 1999 (49) A-2361 M E D I Z I N DIE ÜBERSICHT Senkung der Sectio-Rate von mehr als 30 Prozent geführt haben (28, 32). Der Neugeborenenherpes wird in den USA auf eine von zirka 5 000 Geburten und in England auf eine von 30 000 Geburten geschätzt, für Deutschland sind keine Zahlen bekannt. Ein weiteres Risiko besteht für Neugeborene, deren Mütter keine Antikörper gegen Herpes-simplexViren haben (zirka fünf bis zehn Prozent) und die durch Personal oder durch Besucher oral mit dem Virus infiziert werden. Diese Kinder sind dem Virus schutzlos ausgeliefert, weshalb die Infektion hier in der Regel sehr schwer verläuft. Personal und Besucher mit floridem Herpes labialis beziehungsweise facialis sollten daher nicht ohne Schutzmaßnahmen Neugeborenenstationen betreten. Differentialdiagnose des Herpes genitalis Der primäre Herpes wird wegen der Beschwerden anfänglich nicht selten mit einer Pilzinfektion verwechselt. Gelegentlich bestehen Herpesund Pilzinfektion gleichzeitig. Beim rezidivierenden Herpes genitalis spielt neben der Pilzinfektion das Behçet-Syndrom differentialdiagnostisch eine besondere Rolle (Abbildung 8), da diese mit Ulzera einhergehende Vaskulitis rezidivieren kann, insbesondere in der Schwangerschaft. Wenngleich die Lues selten geworden ist, sollte bei einem Ulkus im Genitalbereich immer auch an eine primäre Lues gedacht werden. Eine lues-serologische Untersuchung sollte durchgeführt werden. Über weitere Differentialdiagnosen informiert der Textkasten Differentialdiagnose. Der genitale Herpes bei Patienten mit Immunschwäche Unter bestimmten Voraussetzungen kommt es zur Dissemination der HSV-Infektion und gelegentlich zum Befall innerer Organe. Diese schweren, teilweise lebensbedrohlichen Her- Diagnostik des Herpes genitalis c Kulturelle Anzüchtung und Typisierung: Dies ist bis heute die Nachweismethode der Wahl, da Herpesviren in der Zellkultur leicht und schnell anzüchtbar sind. Bei hohen Virusmengen ist die Zellkultur nach 24 Stunden schon positiv. Ist nur wenig Virus vorhanden, so kann das Auftreten des zytopathischen Effektes in der Zellkultur einige Tage dauern. Die Bestätigung der Diagnose und die Bestimmung des Virustyps erfolgen durch einen anschließenden Fluoreszenztest unter Verwendung typspezifischer Immunseren. c Direkter Antigentest: Es steht auch ein Fluoreszenztest zum Nachweis von HSV zur Verfügung. Hierzu wird der Abstrich aus dem Blasen-/Ulkusgrund auf einem Objektträger abgerollt und später mit Aceton oder Alkohol fixiert. Diese Methode hat den Vorteil, daß Zellkulturen nicht erforderlich sind und auch Transportprobleme keine Rolle spielen, da das Präparat dauerhaft ist. Die Sensitivität dieser Methode liegt jedoch im Vergleich zur Kultur nur bei 80 bis 95 Prozent. Zusätzlich stehen auch Enzymtests zur Verfügung, deren Sensitivität etwas niedriger ist. c Molekularbiologische DNA-Methoden: Der Nachweis mittels Hybridisierung entspricht in etwa der Sensitivität der Antigennachweise. Die Methoden der Zukunft werden jedoch Amplifikationsmethoden (PCR/LCR) sein. Bisher werden diese bei Verdacht auf Herpesenzephalitis angewendet. Für die Routinediagnostik ist die Methode bis jetzt noch nicht praktikabel etabliert. c Serologie: Der Nachweis von Antikörpern ist weder für die Diagnostik des primären Herpes genitalis noch für das Herpes-genitalis-Rezidiv geeignet. Er ist jedoch wertvoll zur Bestimmung des Immunstatus oder der Unterscheidung zwischen Primärinfektion und Rezidiv. Beim Herpes-genitalis-Rezidiv lassen sich nur in den wenigsten Fällen IgM-spezifische Antikörper nachweisen, so daß auch hier die Serologie nicht hilfreich ist. Viele der kommerziell angebotenen serologischen Tests zur Unterscheidung von Antikörpern gegen HSV 1 und 2 erfüllen die in sie gesetzte Erwartung bis heute nicht. pesinfektionen können außer bei Neugeborenen (Herpes neonatorum, Herpes sepsis), bei Patienten mit schweren Hauterkrankungen wie Dermatitis atopica (Ekzema herpeticatum, varicelliforme Eruption Kaposi), bei Patienten mit kongenitalen und erworbenen Immundefekten wie iatrogene Immunsuppression (Transplantatempfänger), Mangelernährung und bei Aids auftreten (3, 10, 11, 17). Insbesondere bei HIV-Patienten im fortgeschrittenen Stadium mit CD4-Zellzahlen < 100/mm3 treten besonders schwere und atypische Manifestationen der HSV-Infektionen auf. Vom Schweregrad her können Bilder wie bei einem primären Herpes genitalis in Erscheinung treten. A-2362 (50) Deutsches Ärzteblatt 96, Heft 38, 24. September 1999 Das Spektrum der Infektionen mit dem Herpes-simplex-Virus bei HIV-positiven Patienten umfaßt den perianalen Herpes mit riesenhaften Ulzera, den Herpes genitalis, die Herpes-Proktitis, Infektionen des Gesichts, der Nagelumgebung, der Handfläche, die Keratoconjunctivitis, die Herpes-Meningoenzephalitis und die nekrotisierende Retinitis. Persistierende Erosionen, teilweise auch papulöse Proliferationen, die zur Dissemination neigen, werden nachweisbar (14). Genitale Ulzera stellen möglicherweise einen Risikofaktor für den Erwerb und Übertragung von HIV dar (12, 23). Inwiefern Herpesviren wie HSV, CMV und humanes Herpes- M E D I Z I N DIE ÜBERSICHT Tabelle Behandlung der Herpes-simplex-Infektion Virostatikum Arzneiform/ Dosierung/die Dauer Bemerkungen Aciclovir (z. B. Zovirax) Infusion 3 x 5 mg/kg 5 Tage Primärinfektion, schwere Verläufe, auch bei bes. Immunsupprimierten, Primärinfektion, Rezidive Filmtabletten 5 Tage 5 x 200 mg Filmtabletten 6–12 2 x 200 mg–2 x 400 mg Monate häufige Rezidive Valaciclovir Filmtabletten (z. B. Valtrex S) 2 x 500 mg 5–10 Tage Primärinfektion, Rezidive Famciclovir (Famvir) 5 Tage Primärinfektion 5 Tage Rezidive 2–3 Wochen nur bei resistenten HSV-Viren, wenn keine Alternative besteht Foscarnet (z. B. Foscavir) Filmtabletten 3 x 250 mg Filmtabletten 2 x 125 mg Infusion 3 x 40 mg bei Immunsupprimierten virus 6 Kofaktoren bei der HIV-Progression darstellen, ist noch nicht eindeutig geklärt, zumal die meisten Ergebnisse aus In-vitro-Untersuchungen stammen (29). Diagnostik Es gibt eine Reihe diagnostischer Verfahren (1, 6, 7, 24, 26, 27, 30), wobei der Erregernachweis aus Bläschen oder Erosionen beziehungsweise Ulzera der zuverlässigste Weg der Diagnosesicherung ist. Weitere labordiagnostische Verfahren sind dem Textkasten Diagnostik zu entnehmen. Behandlung Zur Therapie und Prophylaxe von Herpes-simplex-Infektionen im Genitalbereich stehen eine Reihe von Virostatika zur Verfügung (Tabelle). 1 Aciclovir (zum Beispiel Zovirax) Aciclovir ist ein Guanosinanalogon, das von mit Herpes infizierten Zellen selektiv aufgenommen wird. Die Herpesviren überführen Aciclovir durch eine viruskodierte Thymidinkinase in das Monophosphat, das anschließend durch zelluläre Enzyme in die aktive antivirale Form, Aciclovir-Triphosphat, umgewandelt wird. Aciclovir-Triphosphat hemmt die virale DNA-Synthese durch Kompetition mit dem natürlichen Desoxyguanosintriphosphat, welches von der viralen DNA-Polymerase für die DNA-Synthese benutzt wird. Die Hemmung der HSV-DNA-Polymerase durch Aciclovir-Triphosphat ist im Vergleich zu Penciclovir-Triphosphat um den Faktor 75 bis 160 stärker. Weiterhin wird Aciclovir-Triphosphat in die virale DNA eingebaut. Schließlich resultiert ein Kettenabbruch in der DNA-Kette, so daß kein funktionsfähiges Genom entstehen kann. 1 Famciclovir (zum Beispiel Famvir) Famciclovir ist ein Pro-Drug, dessen Wirkung erst durch Metabolisierung zum Penciclovir zustande kommt. Die eigentliche virostatische Substanz ist das Penciclovir-Triphosphat, das in analoger Weise wie das Aciclovir in den mit Herpes infizierten Zellen gebildet wird. Die Halb- wertzeit des Famciclovirs ist länger als die von Aciclovir, weshalb weniger Dosen pro Tag gegeben werden. 1 Valaciclovir (zum Beispiel Valtrex S) Valaciclovir ist der Valin-Ester des Aciclovirs und wird nach oraler Aufnahme durch die Valaciclovirhydrolase im Darm und der Leber schnell und nahezu vollständig in Aciclovir und L-Valin umgewandelt. Hierdurch ist eine signifikant verbesserte Bioverfügbarkeit von Valaciclovir (54 Prozent) gegenüber Aciclovir (15 bis 25 Prozent) gegeben. Es lassen sich hierdurch 24stündige Plasmaspiegel erreichen, die bisher nur durch intravenöses Aciclovir zu erzielen waren. Die Wirkung des Valaciclovirs wird durch Aciclovir beziehungsweise Aciclovir-Triphosphat erreicht. Entsprechend ist auch der Wirkungsmechanismus von Valaciclovir. Behandlung des primären Herpes genitalis Die frühzeitige systemische Verabreichung der antiviralen Substanz ist hier entscheidend. Eine mindestens fünftägige Therapie wird empfohlen. In Einzelfällen wird man die Dosis steigern und auch die Therapiedauer verlängern müssen. Bei starker Schmerzsymptomatik sollte für die ersten ein bis drei Tage zusätzlich Diclofenac 100 mg ein- bis zweimal pro Tag verabreicht werden. Auch kann die lokale Verabreichung von anästhesierenden Salben auf den Periurethralbereich eine halbe Stunde vor dem Wasserlassen diesen Vorgang erleichtern. Behandlung des rezidivierenden Herpes genitalis Die Therapie hängt von Ausmaß und Schwere des Rezidivs ab. Die systemische orale Therapie bietet erhebliche Vorteile gegenüber der lokalen Anwendung der antiviralen Substanz. Die Dauer der Behandlung kann hier in vielen Fällen auf ein bis drei Tage beschränkt bleiben. Bei frühzeitigem Therapiebeginn, das heißt bei Auftreten der Prodromalsymptomatik kann Deutsches Ärzteblatt 96, Heft 38, 24. September 1999 (51) A-2363 M E D I Z I N DIE ÜBERSICHT/FÜR SIE REFERIERT die Infektion in vielen Fällen unterdrückt werden, ohne daß es zu größeren Bläschen kommt. Suppressionsbehandlung Bei sehr häufig auftretendem Herpes genitalis gibt es zwei Behandlungsmöglichkeiten: c Die Suppressionsbehandlung, das heißt die tägliche Einnahme der antiviralen Substanz. Dabei muß die Dosis individuell eingestellt werden, indem man die Zahl der Tabletten solange reduziert, wie es noch nicht zu einem wiederholten Rezidiv kommt. Die Suppressionsbehandlung ist bei vielen Patienten mit häufigen, sehr schmerzhaften, nicht vorhersehbaren und oft psychisch stark belastenden Rezidiven die Methode der Wahl. Für die Suppressionstherapie mit Aciclovir liegen Erfahrungen über bis zu zehn Jahre vor (2, 20), für Valaciclovir über bis zu einem Jahr (8). c Die frühzeitige orale Gabe der antiviralen Substanz, wobei der Patient seine Prodromalzeichen oder den Zeitpunkt oder das äußere Ereignis, welches gewöhnlich zur Auslösung des Herpesrezidivs führt, sehr gut kennen muß. Therapie in der Schwangerschaft Eine Teratogenität von Aciclovir wurde in Tierversuchen nicht nachgewiesen. Erfahrungen mit der Aciclovirtherapie von Herpesinfektionen bei schwangeren Frauen sind im internationalen Aciclovir-Schwangerschaftsregister dokumentiert. Weltweit sind nach Orginalherstellerangaben bisher 1 060 Schwangere mit einer Herpesinfektion mit Aciclovir behandelt und ausgewertet worden (Stand: 30. 6. 1997). Demnach besteht kein erhöhtes Risiko an Fehlbildungen nach Aciclovirgabe in der Schwangerschaft. Dennoch besteht für die Therapie einer Herpesinfektion mit Aciclovir in der Schwangerschaft eine relative Kontraindikation, das heißt eine Nutzen-Risiko-Abwägung beziehungsweise strenge Indikationsstellung ist notwendig. Eine Behandlung sollte nur durchgeführt werden bei: c primärem Herpes genitalis in der Schwangerschaft, c Vermeidung einer Sectio caesarea durch prophylaktische Gabe von Aciclovir während der Entbindung, c schwerem Herpes zoster in der Schwangerschaft, c anderen schweren Erkrankungsformen durch HSV und VZV. In der Frühschwangerschaft (1. bis 14. SSW) sollte man aus Gründen der Vorsicht Aciclovir nach Möglichkeit nicht verordnen, da die bisherigen Beobachtungsfälle nicht ausreichen, um jedes Risiko völlig ausschließen zu können. Zitierweise dieses Beitrags: Dt Ärztebl 1999; 96: A-2358–2364 [Heft 38] Die Zahlen in Klammern beziehen sich auf das Literaturverzeichnis, das über den Sonderdruck beim Verfasser und über die Internetseiten (unter http://www.aerzteblatt.de) erhältlich ist. Anschrift für die Verfasser Prof. Dr. med. Eiko E. Petersen Universitäts-Frauenklinik Freiburg Sektion Gynäkologische Infektiologie Hugstetter Straße 55 79106 Freiburg Zigarrenrauchen erhöht Krebs- und KHK-Risiko Bekanntermaßen ist das Zigarrenrauchen mit einer erhöhten Inzidenz von Krebserkrankungen und chronisch obstruktiven Atemwegserkrankungen (COPD) assoziiert. Ob jedoch wie beim Zigarettenrauchen eine Assoziation zu kardiovaskulären Erkrankungen (KHK) besteht, ist bislang nicht untersucht worden. Hierzu legten Autoren aus Kalifornien Daten einer Kohortenstudie mit 17 774 Teilnehmern vor, bei denen 1 546 Zigarrenraucher identifiziert werden konnten. In der Nachbeobachtungszeit von 24 Jahren zeigte sich ein relatives Risiko von 1,27 für das Auftreten einer KHK, das Risiko für die COPD stieg auf das 1,45fa- che, das für Karzinome des oberen Respirationstrakts auf das 2,02fache und das des unteren Respirationstrakts auf das 2,14fache. Wie beim Zigarettenrauchen auch ließ sich ein Synergismus von Zigarrenrauchen und Alkoholkonsum bezüglich des Auftretens von oropharyngealen und broncho-ösophagealen Tumoren nachweisen. acc Iribarren C et al.: Effect of cigar smoking on the risk of cardiovascular disease, chronic obstructive pulmonary disease, and cancer in men. N Eng J Med 1999; 340: 1773–1780. Dr. Iribarren, Division of Research, Kaiser Permanente Medical Care Program, 3505 Broadway, Oakland, CA 947611, USA. Lymphknotendissektion beim Magenkarzinom Die kurative Resektion gilt nach wie vor als einzige Möglichkeit, beim Magenkarzinom eine Heilung zu erreichen. Kontrovers wird derzeit das Ausmaß der hierfür erforderlichen Lymphknotendissektion diskutiert, wobei die ausgedehnte Dissektion (Kompartiment D2) oder die eingeschränkte Dissektion (D1) möglich sind. Eine kontrollierte Studie untersuchte an 711 Patienten mit Magenkarzinom, welcher Behandlungsansatz bessere Ergebnisse hinsichtlich Morbidität, postoperativer Mortalität, Langzeitüberleben und Rezidivrate ergab. Die Komplikationsrate war in der D2-Gruppe mit 43 Prozent signifikant höher als in der D1-Gruppe mit 25 Prozent, ebenso zeigte sich eine erhöhte A-2364 (52) Deutsches Ärzteblatt 96, Heft 38, 24. September 1999 postoperative Mortalität (zehn versus vier Prozent). Bei der Rezidivrate schnitt die radikaler operierte Gruppe geringfügig besser ab als die restriktiv behandelte Gruppe (37 versus 43 Prozent), bei den Fünf-Jahres-Überlebensraten fanden sich dagegen keine Unterschiede. Aufgrund dieser Ergebnisse empfehlen die Autoren, der eingeschränkten Lymphknotenresektion beim Magenkarzinom den Vorzug zu geben. acc Bonenkamp JJ, Hermans J, Sasako M, van de Velde CJH: Extended lymph-node dissection for gastric cancer. N Eng J Med 1999; 340: 908–914. Prof. van de Velde, Department of Surgery, Leiden University Medical Center, PO Box 9600, 2300 RC Leiden, Niederlande.