NOBAGLOVE ®
Transcription
NOBAGLOVE ®
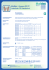
® NOBAGLOVE -Cytostax Größe XS, S, M, L und XL, blau, 290 mm Produktbeschreibung und Zweckbestimmung Einmal-Produkt mit Doppelfunktion als Schutzhandschuh nach PSA und medizinischer Untersuchungshandschuh, puderfrei, zum Schutz vor pathogenen Keimen. Er ist vor allem beim Umgang mit Zytostatika in der Medizin und im Labor geeignet. NOBAGLOVE® -Cytostax sind anatomisch geformt, mit extra langer Stulpe und Rollrand ausgerüstet und hypoallergen. Die Handschuhe sind im Fingerbereich 0,14 mm dick und auch geeignet für „double gloving“. Zusammensetzung Butadiennitrilkautschukpolymer Hilfsmittel: Zink-Di-n-Dibutyl-Dithiocarbamat Es enthält keinen Thioharnstoff und kein Mercapto-benzothiazol. Das Produkt ist chloriniert und latexfrei. Normative und gesetzliche Anforderungen NOBAGLOVE® –Cytostax ist ein Medizinprodukt nach MPG, Klasse I, Regel 5 und erfüllt die Anforderungen der Richtlinie 93/42/EWG, der EN 455 1-4 (Medizinische Handschuhe zum einmaligen Gebrauch), sowie der EN 1186 (Werkstoffe und Gegenstände in Kontakt mit Lebensmitteln). Ebenso den ASTM D 6319 Standard (Standard Spezifikation für Nitril Untersuchungshandschuhe für Medizinische Anwendungen). Die Handschuhe erfüllen die Normen der PSA (Cat. III) nach EN 420 (Schutzhandschuhe), der EN 374 (Schutzhandschuhe gegen Chemikalien und Mikroorganismen) sowie der EN 388 (Schutzhandschuhe gegen mechanische Risiken). Sie wurden zusätzlich speziell nach ASTM D 6978-05 auf die Durchdringung von Chemotherapeutika getestet, die schon bei 0,01 µg/cm2/min den Durchbruch misst (Standard Practice for Assessment of Resistance of Medical Gloves to Permeation by Chemotherapy Drugs). Die Virendichtigkeit ist geprüft und erfüllt ASTM F 1671-97b. Der AQL ist 1,5 in Bezug auf die Dichtheit (ISO 2859-1). Die Puderbestimmung erfolgt nach EN 455 / EN ISO 21171. Der Pudergehalt liegt unter dem normativ vorgegeben Grenzwert von max. 2 mg/Handschuh. Das Produkt enthält keine gefährlichen toxischen Substanzen gemäß REACH. Es trägt CE– und DIN EN ISO 15223-1– Kennzeichnung auf allen Verpackungsstufen. Verpackung Primärverpackung: Sekundärverpackung: Faltschachtel aus Zellulose Karton aus Zellulose Lagerung Trocken und staubfrei zwischen +5°C und +40°C lagern, vor direkter Sonneneinstrahlung schützen Stand der Information: 09.12.2013 [REV 2] 2 Blätter ersetzt: 17.10.2013 Durchbruchzeiten Chemikalien nach EN 374-3 Aceton Ammoniumhydroxid 25% Chlorhexidin 4% Essigsäure 10% Ethanol 35 % Ethidiumbromid 1% Formaldehyd 35% Formalin 10 % Glutaraldehyd 5% Isopropanol Isopropylalkohol 70 % Natriumhydroxid 30% Natriumhydroxid 40% n-Heptan n-Hexan Salpetersäure 36% Salzsäure 36 % Wasserstoffperoxid 3% Level 1 >10 min Level 4 >120min Level 2 >30 min Level 5 >240min Level 0 Level 0 6-12’ Level 6 Level 4 Level 1 16-22’ Level 6 Level 4 Level 6 Level 6 Level 0 Level 1 Level 6 Level 6 Level 0 Level 0 Level 2 Level 3 Level 6 Level 3 >60 min Level 6 >480min Je nach Arbeitsplatzbedingungen kann die tatsächliche Schutzdauer von den Werten der Tabelle abweichen. Vor Gebrauch auf Schäden kontrollieren. Beschädigte Handschuhe nicht verwenden. Wiederaufbereitung nicht möglich. Entsorgung entsprechend den geltenden Vorschriften. CE 0321, PPE (cat. III), SATRA Technology Centre, Wyndham Way, Telford Way, Kettering, Northamptonshire, NN16 8SD United Kingdom. Durchbruchzeiten Chemotherapeutika nach ASTM D 6978-5 Carmustin 3,3 mg/ml, 3300 ppm Cisplatin 1,0 mg/ml, 1000 ppm Cyclophosphamid 20 mg/ml, 20000ppm Dacarbazin 10 mg/ml, 10000ppm Doxorubicin 2,0 mg/ml, 2000 ppm Etoposid 20 mg/ml, 20000 ppm Fluorouracil 50 mg/ ml, 50000 ppm Methotrexat 25 mg/ml, 25000 ppm Mitomycin C 0,5 mg/ml, 500 ppm Paclitaxel 6,0 mg/ ml, 6000 ppm Thiotepa 10 mg/ml, 10000 ppm Vincristin Sulfat 1,0 mg/ml, 1000 ppm ≤ 15-30‘ ≤ 240’ ≤ 240’ ≤ 240’ ≤ 240’ ≤ 240’ ≤ 240’ ≤ 240’ ≤ 240’ ≤ 240’ ≤ 30-45’ ≤ 240’ Wir weisen darauf hin, dass auch bei intaktem Handschuh ein mindestens stündlicher Wechsel bei der Verwendung mit Zytostatika unabhängig von Durchbruchzeiten größer 60 Minuten in den einschlägigen Richtlinien empfohlen wird. Stand der Information: 09.12.2013 [REV 2] 2 Blätter ersetzt: 17.10.2013 NOBAGLOVE®-Cytostax size XS, S, M, L and XL, blue, 290 mm Product Description and Purpose The disposable product has a dual function as protective glove in compliance with PPE and as medical examination gloves, powderfree, suited for protection against pathogenic germs. They are qualified in particular for handling cytostatics in medicine and in the laboratory. NOBAGLOVE®Cytostax, anatomically shaped, is provided with extra long, rolled cuffs. They are hypoallergenic. The thickness of the finger area is 0.14 mm. The gloves are also suited for “double gloving”. Composition Butadiene nitrile rubber polymer Auxiliaries: zinc di-n-dibutyl-dithiocarbamate The product is chlorinated and latex-free. It does not contain thiourea or mercaptobenzothiazole. Normative and Legal Requirements NOBAGLOVE®–Cytostax is a medical product in accordance with the MDD, class I, rule 5, and complies with the requirements of the directive 93/42/EEC, of EN 455 1-4 (Single use medical gloves), as well as EN 1186 (Materials and articles in contact with foodstuffs), also complying with standard ASTM D 6319 (Standard Specification for Nitrile Examination Gloves for Medical Application). The gloves comply with the standards of Personal Protective Equipment (Cat. III) in accordance with EN 420 (Protective Gloves), with EN 374 (Gloves Giving Protection from Chemicals and MicroOrganisms), and with EN 388 (gloves Giving Protection from Mechanical Risks). In addition, they have been specially tested in accordance with ASTM D 6978-05 as to the breakthrough detection time of chemotherapeutics, which measures already at 0.01 μg/cm2/min the breakthrough (Standard Practice for Assessment of Resistance of Medical Gloves to Permeation by Chemotherapy Drugs). The virus imperviousness is tested and complies with ASTM F1671-97b. The AQL is ≤ 1.5 referring to the imperviousness (ISO 2859-1). The powder content is ascertained according to EN 455 / EN ISO 21171. The powder content is below the maximum permissible normative value of 2 mg/glove. The product does not contain dangerous toxic substances according to REACH. It has CE marking and DIN EN ISO 15223-1 labels on all its packaging. Packaging Primary packaging: folding box made of cellulose Secondary packaging: carton made of cellulose Storage To be stored in a dry and dust-free environment between +5°C and +40°C, protected against direct sunlight Stand der Information: 09.12.2013 [REV 2] 2 Blätter ersetzt: 17.10.2013 Breakthrough Times of Chemicals according to EN 374-3 Breakthrough Times of Chemotherapeutics according to ASTM D 6978-5 Acetone Ammonium Hydroxide 25% Chlorhexidine 4% Acetic Acid 10% Ethanol 35 % Carmustine 3.3 mg/ml, 3300 ppm Cisplatin 1.0 mg/ml, 1000 ppm Cyclophosphamide 20 mg/ml, 20000ppm Dacarbazine 10 mg/ml, 10000ppm Doxorubicin 2.0 mg/ml, 2000 ppm Etoposide 20 mg/ml, 20000 ppm Fluorouracil 50 mg/ml, 50000 ppm Methotrexate 25 mg/ml, 25000 ppm Mitomycin C 0.5 mg/ml, 500 ppm Paclitaxel 6.0 mg/ ml, 6000 ppm Thiotepa 10 mg/ml, 10000 ppm Vincristine Sulfate 1.0 mg/ml, 1000 ppm . Ethidiumbromide 1% Formaldehyde 35% Formalin 10 % Glutaraldehyde 5% Isopropanol Isopropyl Alcohol 70 % Natriumhydroxide 30% Natriumhydroxide 40% n-Heptane n-Hexane Nitric Acid 36% Hydrochloric Acid 36 % Hydrogen Peroxide 3% Level 1 >10 min Level 4 >120min Level 2 >30 min Level 5 >240 min Level 0 Level 0 6-12’ Level 6 Level 4 Level 1 16-22’ Level 6 Level 4 Level 6 Level 6 Level 0 Level 1 Level 6 Level 6 Level 0 Level 0 Level 2 Level 3 Level 6 Level 3 >60 min Level 6 >480 min Depending on the working conditions, the actual duration of protection may differ from the values in the table. Check for damage before use. Do not use damaged gloves. No reprocessing. Disposal in accordance with legislation in force. CE 0321, PPE (cat. III), SATRA Technology Centre, Wyndham Way, Telford Way, Kettering, Northamptonshire, NN16 8SD United Kingdom. ≤ 15-30‘ ≤ 240’ ≤ 240’ ≤ 240’ ≤ 240’ ≤ 240’ ≤ 240’ ≤ 240’ ≤ 240’ ≤ 240’ ≤ 30-45’ ≤ 240’ Please note that even intact gloves should be changed at least every hour, if used with cytostatics regardless of breakthrough times exceeding 60 minutes, according to the relevant directives. Stand der Information: 09.12.2013 [REV 2] 2 Blätter ersetzt: 17.10.2013