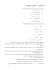הצבר הקנוני
Transcription
הצבר הקנוני
הצבר הקנוני
30.4.15
1
הצבר הקנוני
נעבוד בצבר הקנוני כדי לתאר מערכת שבה הטמפרטורה ,Tמספר החלקיקים Nוהנפח Vקבועים .ניתן לשמור
על טמפרטורה קבועה במערכת על ידי צימודה למאגר חום בטמפרטורה .Tאנרגיה יכולה לעבור בינה לבין מאגר
החום ולכן הטמפרטורות שלהם משתוות .למאגר חום מושלם קיבול חום אינסופי ,ולכן כאשר האנרגיה שלו משתנה
כתוצאה ממעבר אנרגיה בינו לבין המערכת ,הטמפרטורה שלו נותרת ללא שינוי.
המערכת +מאגר החום מהווים מערכת סגורה ,כלומר מיקרוקנונית .בשיווי משקל ,האנטרופיה של המערכת
הכוללת )מערכת+מאגר( מקסימלית .ניתן להראות שמקסימום אנטרופיה במערכת הכוללת שקול למינימום של
האנרגיה החופשית של הלמהולץ עבור המערכת )הנמצאת בטמפרטורה קבועה ,כלומר בצבר הקנוני( .לכן במערכת
בצבר הקנוני ,בשיווי משקל האנרגיה החופשית של הלמהולץ F = E − T Sמינימלית .משמעות הדבר היא
שבטמפרטורה אפס F = Eולכן האנרגיה מינימלית ,ואילו בטמפרטורה גבוהה F ≈ −T S ,ולכן האנטרופיה
מקסימלית.
−βEi
הקנוני
בצבר
ההסתברות למצוא את המערכת במצב מיקרוסקופי ספציפי iעם אנרגיה Eiהיא ,P (i) = e Z
P
= Zהיא פונקצית החלוקה הקנונית )המסומנת גם ,(QNו־ .β = kB1T
כאשר e−βEi
i∈states
פתרון בעיות בצבר הקנוני:
.1מחשבים את פונקצית החלוקה e−βEi
P
=.Z
i∈states
.2מפונקצית החלוקה ניתן לחשב את:
)א( האנרגיה החופשיתF = − β1 log Z :
∂
= − ∂β
)ב( האנרגיה(log Z) :
∂
) ∂β (βF
=E
2 ∂F
S = − ∂F
)ג( האנטרופיה∂T = kB β ∂β :
= −kB β 2 ∂E
)ד( קיבול החום∂β :
2
∂E
∂T
= CV
מערכת שני מצבים בצבר הקנוני
נחזור לדון במערכת של Nחלקיקים ברי הבחנה שלכל אחד מהם שני מצבים :מצב 0לו אנרגיה ,0ומצב 1לו
אנרגיה .כעת נחקור אותה בצבר הקנוני.
נסמן ב si ∈ 0, 1את מצב החלקיק ה־ .iנשים לב שאנרגית החלקיק ה־ iהיא .Ei = si
ראשית ,פונקצית החלוקה החד־חלקיקית:
e−βs1 = 1 + e−β
X
= Z1
s1 =0,1
ההסתברות של חלקיק להיות במצב ,P (0) = Z11 :0ההסתברות של חלקיק להיות במצב :1
N
P
=H
בחזרה למערכת של Nחלקיקים .ההמילטוניאן של המערכתsi :
i=1
1
e−β
Z1
= ).P (1
פונקצית החלוקה של המערכת:
N
= Z1N = 1 + e−β
N
e−βs1
X
si
=
N
P
−β
e
i=1
s1 =0,1
X
=Z
} {si
האנרגיה החופשית:
1
N
log Z = − log 1 + e−β
β
β
F =−
האנרגיה הפנימית:
e−β
1
)∂(log Z
= N
= N β
∂β
1 + e−β
e +1
E=−
∂S
. T1 = ∂E
ניתן להפוך את הקשר ולקבל את ) T (E־ הזהה לביטוי שחישבנו בצבר המיקרוקנוני מתוך
מכיוון ש־ ,E = N1כאשר N1הוא מספר החלקיקים הממוצע ברמה העליונה ,מהאנרגיה הפנימית הממוצעת
e−β
.N1 = E = N 1+eלחילופין ,ניתן היה לחשב את N1מתוך ) P (1שחושב קודם:
שחישבנו ניתן להסיק ש−β :
מכיוון שאין אינטראקציה בין החלקיקים והם בלתי תלויים ,מספר החלקיקים הממוצע ברמה העליונה שווה
למספר החלקיקים הכולל כפול ההסתברות שחלקיק בודד נמצא ברמה העליונה:
e−β
1 + e−β
N1 = N P (1) = N
בגבול של טמפרטורות נמוכות .E → 0 :(β → ∞) T → 0כל החלקיקים נמצאים במצב 0־ המערכת במצב
עם אנרגיה מינימלית.
בגבול של טמפרטורות גבוהות ∞ → ,E → 12 N :(β → 0) Tכלומר חצי מהחלקיקים נמצאים ברמת
האנרגיה הגבוהה וחצי בנמוכה .כפי שראינו בתרגול שעבר ,זהו המצב של מקסימום אנטרופיה )בו למערכת מספר
רב ביותר של מצבים מיקרוסקופיים(.
קיבול החום:
∂E
∂E
eβ
= −β 2 kB
= kB N β 2 2 β
∂T
∂β
(e + 1)2
2
= CV
בגבולות של טמפרטורות נמוכות וגבוהות קיבול החום שואף לאפס .בטמפרטורה נמוכה רוב החלקיקים נמצאים
ברמת היסוד .כל עוד << ,kB Tשינויים בטמפרטורה לא גורמים לשינוי גדול באנרגיה .בטמפרטורות גבוהות,
כמעט חצי מהחלקיקים ברמת האנרגיה הגבוהה .לא נותרו הרבה חלקיקים ברמת האנרגיה הנמוכה שיכולים
לעבור לגבוהה עם העלאת הטמפרטורה ,ולכן השינוי באנרגיה כאשר מגדילים את הטמפרטורה קטן .קיבול החום
מקסימלי כאשר , ∼ kB Tאז העלאה של הטמפרטורה גורמת לחלקיקים רבים לבצע את הקפיצה הדרושה של
באנרגיה על מנת לעבור מהרמה התחתונה לרמה העליונה.
3
דרגות חופש פנימיות בגז אידיאלי בצבר הקנוני
עד כה דיברנו על גז אידאלי המורכב מיחידות אטומיות ,כלומר התעלמנו מהמצבים הפנימיים של יחידות הגז
)מולקולות באופן כללי( .בתרגול זה נראה מה ההשפעה של דרגות חופש פנימיות בדידות .אלה מופיעות כאשר
מתייחסים למולקולות כאובייקטים קוונטיים ,ולכן המצבים האפשריים שלהן ־ ורמות האנרגיה המתאימות ־
מקוונטטים .החשיבות של חשבון זה הוא עמוק יותר מהסבר של ניסויים מסויימים ־ קלאסית יש רצף של מצבים
פנימיים מסוגים שונים )כגון מרחק בין אטומים במולקולה ,מיקום האלקטרונים באטום ,מיקום חלקי גרעין האטום
אחד ביחס לשני( ,ולכן לפי חוק החלוקה השווה דרגות חופש פנימיות אלה אמורות לתרום הרבה מאוד לאנרגיה
הפנימית והחישובים שעשינו עבור גז אידאלי אינם רלבנטיים .העובדה שהמצבים ורמות האנרגיה בדידים ־ בגלל
מכניקת הקוונטים ־ מסבירה ,כפי שנראה בתרגול ,מדוע לא צריך לקחת בחשבון את כל דרגות החופש בחשבון
)ואילו דרגות חופש כן צריך(.
3.1
פונקציית החלוקה של גז אידאלי קנוני
נזכר ראשית כיצד מחשבים את פונקציית החלוקה של גז אידאלי בצבר הקנוני .ההימלטוניאן של גז אידאלי הוא
P p2i
= Hולכן פוקציית החלוקה מתקבלת על ידי
כרגיל 2m
i
ˆ
)dp3N dq 3N e−βH(p,q
)(1
1
N !h3N
"
#
∞ ˆ
N
p2i,j
VN Y Y
dpi,j exp −β
∞N !h3N i=1 j=x,y,z −
2m
r
N
VN Y Y
2πm
3N
N !h i=1 j=x,y,z
β
N
3N/2
V N 2πm
1
V
≡
N ! h2 β
N ! λ3T
3
=
=
=
=
Z
כאשר הגדרנו את אורך הגל התרמי
h2 β
h
√=
2πm
2πmkB T
r
≡ λT
בהנתן פונקציית החלוקה ,אפשר למצוא את האנרגיה החופשית
2
3
h β
V
− log
+1
F = −kB T log Z = −N kB T log
N
2
2πm
וממנה אפשר לגזור את הגדלים הפיסיקליים המעניינים כמו למשל אנרגיה ממוצעת
)∂ (log Z
) ∂ (βF
=
∂β
∂β
3N
3
= N kB T
2β
2
−
=
E
=
ואת קיבול החום
3
∂E
= N kB
∂T
2
3.2
= CV
דרגת חופש פנימית עם שני מצבים
כעת נניח שלכל מולקולה בגז יש שני מצבים אפשריים אשר נבדלים זה מזה באנרגיה ב )לדוגמה ,מצבים שונים
עבור האלקטרונים ,או קונפורמציות שונות של המולקולה( .כלומר ,ההמילטוניאן ניתן על ידי
si
N
X
i=1
+
N
X
|pi |2
2m
=H
i=1
כאשר siהוא משתנה בינארי )שווה 0או (1המסמל אם המולקולה ה iנמצאת במצב הנמוך יותר אנרגטית )(si = 0
או במצב הגבוה יותר אנרגטית ) .(si = 1עתה פונקציית החלוקה תנתן על ידי הנוסחה
ˆ X
1
)dp3N dq 3N e−βH(p,q,s
N !h3N s ..s
N
=
Z
1
הסכום הוא על כל האפשרויות של Nהמשתנים siלהיות 0או .1
חישוב פונקציית החלוקה
אם נציב את ההמילטוניאן נקבל
"
!#
ˆ X
X |pi |2
X
1
3N
3N
=
dp dq exp −β
+
si
N !h3N s ..s
2m
i
i
1
N
(
"
( )#
"
)#
ˆ
X
X
X |pi |2
1
=
exp −β
si
×
dp3N dq 3N exp −β
)(2
3N
N
!h
2m
s ..s
i
i
N
4
1
Z
איור :1קיבול החום כפונקצייה של טמפרטורה בגז אידאלי עם דרגת חופש פנימית ) (aבינארית )שני מצבים(; )(b
עם n = 10מצבים ו ) (cעם ∞ מצבים
כלומר ,פונקציית החלוקה היא מכפלה של פונקציית חלוקה של גז אידאלי ושל מערכת שני המצבים .התפרקות
פונקציית החלוקה למכפלה של של פונקציות חלוקה על תת מערכות )שבמקרה זה שתיהן מוגדרות על אותם
Nחלקיקים!( נובעת מחוסר האינטראקציה בהמילטוניאן בין המערכות ,ולכן הינה כללית )תחת הנחת חוסר
אינטראקציה( .אילו היינו עובדים בצבר המיקרוקנוני היינו רואים ששם אי אפשר לרשום את מספר המצבים בתור
מכפלה )בדיוק( של איבר המתאים לגז אידאלי ואיבר המתאים לדרגת החופש הפנימית ,ולכן החשבון קשה יותר ־
זה )אי התלות בין "חלקי" המערכת( הוא היתרון החישובי של האנסמבל הקנוני על פני המיקרוקנוני.
הסכום ב) (2מחושב כ
"
#
!N
X
X
X
exp −β
si
=
] exp [−βs1
s1 =0,1
N
)(3
)](1 + exp [−β
s1 ..sN
i
=
הסכום הזה הוא פונקצית החלוקה של מערכת 2רמות ,אותה חישבנו קודם.
ואם נשתמש בתוצאה ) (1מהסעיף הקודם נקבל
N
)(4
1 + e−β
N
V
λ3T
1
!N
=Z
קיבול חום
עתה נמצא את האנרגיה החופשית וקיבול החום
−kB T log Z
2
V
3
h β
−β
−N kB T log
− log
+ 1 + log 1 + e
N
2
2πm
ולכן האנרגיה הממוצעת היא
) ∂ (βF
∂β
3
e−β
N kB T + N
2
1 + e−β
5
=
=
E
=
=
F
וקיבול החום הוא
−β
+ 2 e−2β
−2 e−β 1 + e
3
N kB + N
2
=
3
e−β
N kB + N kB β 2 2
2
2
) (1 + e−β
=
2
) (1 + e−β
)(5
∂β
∂T
CV
∂β
. ∂T
כאשר השתמשנו בעובדה ש = − kB1T 2 = −kB β 2
הבה ננתח את התנהגות קיבול החום עבור טמפרטורות נמוכות וגבוהות :עבור β → ∞ ,T → 0ולכן
e−β → 0ואנו מקבלים .CV (T → 0) → 23 N kBעבור ∞ → β → 0 ,Tולכן e−β → 1ואנו מקבלים
.CV (T → ∞) → 32 N kBהאם מכאן ניתן ללמוד שדרגות החופש הפנימיות לא משפיעות? אם מציירים במחשב
את קיבול החום כפונקציה של טמפרטורה ,כמו באיור ,1aמקבלים מקסימום באזור הערך .β ∼ 1ההתנהגות
הלא מונוטונית של קיבול החום נקראת "אנומליית שוטקי" והיא נמדדה ניסויית )בעיקר במוצקים ולא בגזים ,אבל
הסיבה היא זהה( .מקסימום צר של קיבול החום משמעו דרגות חופש חסומות )כלומר ,עם אנרגיה מקסימלית( שלא
מעוררות מתחת לטמפרטורה מסויימת ,ורוויות מעל לטמפרטורה אחרת .מכאן אפשר ללמוד שבחשבון יש לקחת
רק דרגות חופש רלבנטיות ,כלומר שהאנרגיה שלהן , ∼ kB Tודרגות חופש עם אנרגיה גדולה בהרבה או קטנה
בהרבה אפשר להזניח.
חישוב בצבר המיקרו קנוני
מלבד הרלבנטיות הפיסיקלית של מערכת זו ,זו גם דוגמה הממחישה את היתרון של הצבר הקנוני על פני
המיקרוקנוני.
4
4.1
דרגת חופש פנימית בדידה
מולקולה עם nמצבים פנימיים
אילו למולקולת הגז היו nמצבים אפשריים במקום רק שניים )אם לוקחים בחשבון עוד רמות אנרגיה אפשריות,
או יותק קונפורציות של המולקולה( ,כל שהיה משתנה הוא שהסכום ) (3היה על nהמצבים .לשם הפשטות נניח
שהאנרגיה של המצב ה kהיא .kאז
]1 − exp [−βn
]1 − exp [−β
=
] exp [−βs1
n−1
X
s1 =0
ולכן פונקציית החלוקה היתה
N
)(6
]1 − exp [−βn
]1 − exp [−β
N
V
λ3T
1
!N
=Z
אם נחשב את קיבול החום כעת נקבל כמו באיור ,1bשרוחב המקסימום גדל מכיוון שיש תחום גדול יותר של
טמפרטורות עבורו יש רמות חדשות לעורר .עם זאת ,עבור טמפרטורה גבוהה מספיק קיבול החום יחזור לערך של
גז אידאלי רגיל )כלומר ,נראה אנומליית שוטקי(.
4.2
מולקולה עם ∞ מצבים פנימיים
באותה שיטה ניתן לחשב את קיבול החום כאשר יש אינסוף מצבים עבור דרגת החופש הפנימית )עם הפרש אנרגיה
קבוע ( .זהו המצב עבור מולקולה דו אטומית שממודלת כקפיץ קוונטי .במצב כזה הסכום יהיה
6
1
]1 − exp [−β
] exp [−βs1
=
∞
X
s1 =0
ולכן
)(7
N
−N
)](1 − exp [−β
V
λ3T
1
=Z
!N
קיבול החום במקרה זה הוא
!
2
)e−β (β
3
+
2 (1 − e−β )2
CV = N kB
והוא מופיע באיור .1cכפי שניתן לראות במקרה זה ,אין מקסימום צר בקיבול החום אלא יש עלייה מונוטונית
מהערך CV = 23המתאים לגז אידאלי ללא דרגות חופש פנימיות ,לערך CV = 25המתאים לגז אידאלי של קפיצים
)חד מימדיים ,שאינם יכולים להסתובב ־ כמו בתרגיל הבית( .שימו לב שהגרף מתאר התנהגות קוונטית ,מכיוון שרק
קוונטית יש רמות אנרגיה בדידות ,שאינן מעוררות בטמפרטורות נמוכות מספיק .קלאסית )כפי שתמצאו בתרגיל
הבית( דרגות החופש הפנימיות )בעלות אנרגיה רציפה( מעוררות בכל טמפרטורה גדולה מאפס .גרף מהסוג הזה
אכן נמדד בניסוי ומהווה אישוש למכניקת הקוונטים!
7